Pterígio
El Pterígio ou carnosidade no olho é um crescimento anormal da conjuntiva (membrana transparente do olho) na direção da córnea, às vezes, pode cobrir. Em geral o pterígio aparece na cavidade nasal ou dentro do olho, Embora também pode aparecer do lado de fora.
El tratamento de pterígio abrange desde colírio lubrificante no primeiros estados para cirurgia de pterígio em casos mais avançados.
Pterígio
El Pterígio ou carnosidade no olho é um crescimento anormal da conjuntiva (membrana transparente do olho) na direção da córnea, às vezes, pode cobrir. Em geral o pterígio aparece na cavidade nasal ou dentro do olho, Embora também pode aparecer do lado de fora.
El tratamento de pterígio abrange desde colírio lubrificante no primeiros estados para cirurgia de pterígio em casos mais avançados.
O que é o pterígio?
El pterígio, às vezes também escrito como pterígio, é uma lesão neoplásica benigna caracterizada por um crescimento fibrovascular local invasivo da conjuntiva em direção à córnea (1).
El origem desse tecido proliferativo está na células-tronco epiteliais basais do leito límbico (CMEL) que são ativados e transformados em tecido conjuntivo (2).
Causas do pterígio
Foi demonstrado que O principal fator de ativação causador do pterígio é a radiação ultravioletaPortanto, sua incidência é muito maior nos países da faixa equatorial com alta taxa de insolação (3-6). Embora tenha sido proposto uma vez, não parece haver uma predisposição genética para pterígio (7).
A radiação UV solar atuaria na área temporal do olho, espalhando-se pela córnea, como se fosse através de um espelho duplo formado pelo epitélio e pelo endotélio, atingindo a região nasal com efeito potencializador de até 20 vezes maior no área de saída, nasal, em relação à entrada, temporal (8). Por ele, a lesão começa nesta área nasal, que é mais protegida do sol, o que parece uma contradição.
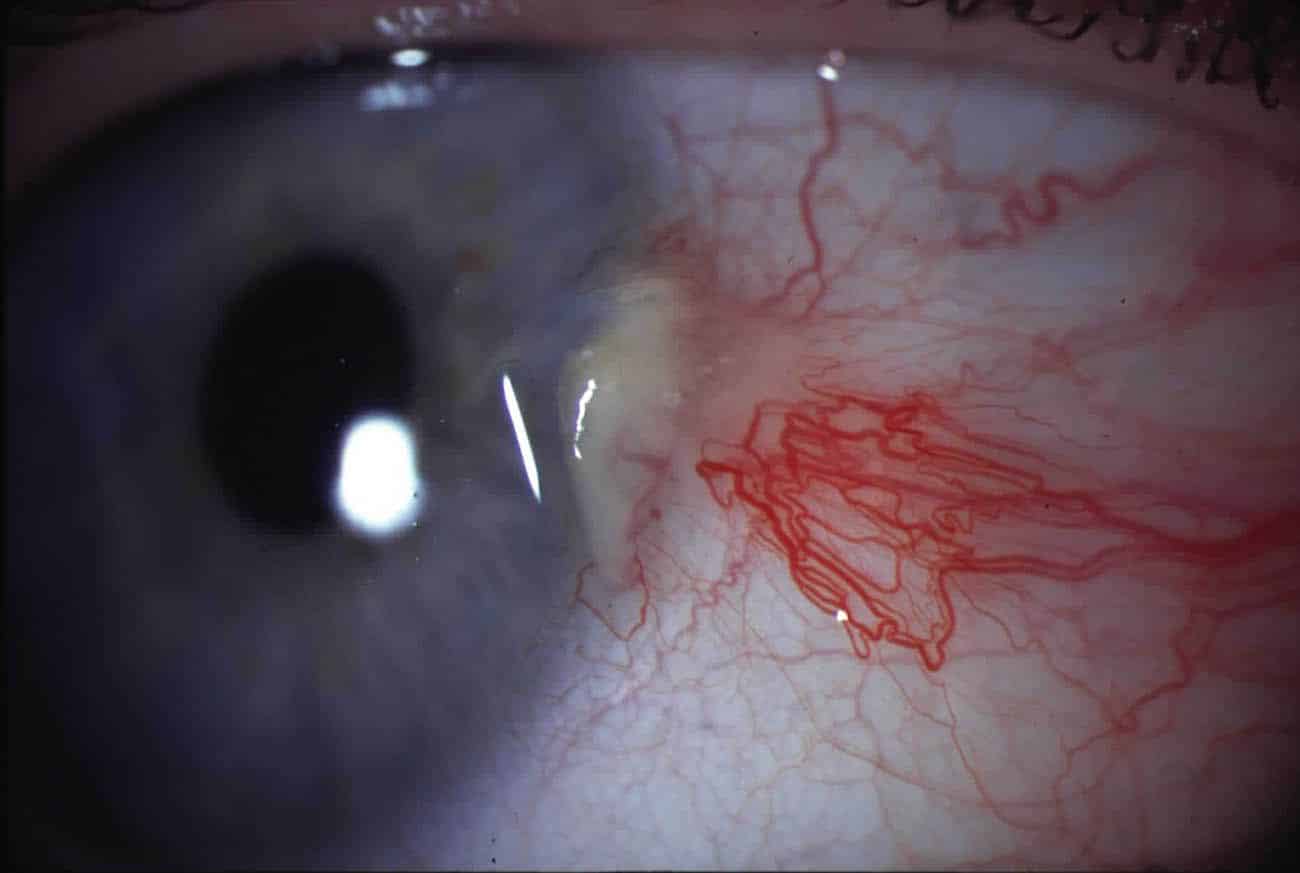
El O primeiro efeito dos raios ultravioleta nos tecidos é uma degeneração elástica da substância própria subconjuntival.. UV ativa fibroblastos que geram elastina anormal que não pode mais ser degradada pela elastase (9,10). A elastina anômala se acumulará até dar uma imagem de lesão redonda, sobreelevado y aparência amarelada localizada na área nasal perto do limbo, este é o que chamamos pinguecula (Figura 3).
A este processo degenerativo está associado um reação inflamatória responsável pelo aparecimento de vasos sanguíneos no espaço subconjuntival, circundando a lesão e formando um feixe fibrovascular de formato triangular com ápice em direção à córneao que levará ao pterígio.
Estudos histoquímicos e de biologia molecular mostram que no pterígio os ELSCs expressam a mutação de um gene supressor de tumor que causa a presença da proteína p53 (11,12), um marcador comum em diversos cânceres humanos e em lesões actínicas do pterígio. (13), o que sugere que o Pterígio seria um distúrbio proliferativo semelhante a um tumor. O gene p53 está relacionado aos mecanismos de morte celular programada.
raios ultravioletas agem em CMEL causando uma mutação no gene responsável pela síntese da proteína p53, o gene perde a capacidade de atuar como um fator de transcrição, resultando em proliferação celular descontrolada e uma mudança nos sinais que ativam os fatores de crescimento e a via ciclina D1-Cdk4 (11,12). A consequência da mutação do gene p53 é que os CMEL crescem sem controle (14), tornam-se migratórios e invadem a córnea através da membrana basal (15), arrastando células conjuntivais e induzindo a formação de tecido fibrovascular neste nível, devido à aumento dos níveis de mediadores inflamatórios, fatores proliferativos e angiogênicos, conforme encontrado na análise histopatológica e histoquímica (16).

raios ultravioletas agem em CMEL causando uma mutação no gene responsável pela síntese da proteína p53, o gene perde a capacidade de atuar como um fator de transcrição, resultando em proliferação celular descontrolada e uma mudança nos sinais que ativam os fatores de crescimento e a via ciclina D1-Cdk4 (11,12). A consequência da mutação do gene p53 é que os CMEL crescem sem controle (14), tornam-se migratórios e invadem a córnea através da membrana basal (15), arrastando células conjuntivais e induzindo a formação de tecido fibrovascular neste nível, devido à aumento dos níveis de mediadores inflamatórios, fatores proliferativos e angiogênicos, conforme encontrado na análise histopatológica e histoquímica (16).
Esses estudos revelam, por sua vez, que as alterações ocorrem na "cabeça" do pterígio, região que avança em direção à córnea, sendo muito mais baixa no restante da lesão, dado fundamental a se ter cuidados especiais no tratamento cirúrgico do pterígio. Toda a "cabeça" deve ser bem retirada para eliminar os mediadores responsáveis pelo avanço do pterígio, que causam recidivas frequentes após a cirurgia..
Quando o tecido fibrovascular atinge a córnea o equilíbrio entre metaloproteinase de matriz (MMPs) e inibidores dessas enzimas é perturbado. A concentração de MMPs está aumentada (17), principalmente na cabeça do pterígio, induzindo alterações na estrutura do colágeno da membrana basal do epitélio corneano, da membrana de Bowmann e do estroma corneano. enfraquecimento da estrutura de colágeno facilitando a penetração do tecido fibrovascular do limbo para a córnea (18). Uma vez que a barreira da córnea é enfraquecida, o avanço do tecido fibrovascular é produzido pela presença de fatores inflamatórios, citocinas e fatores pró-angiogênicos (especialmente presença de VEGF) e fatores de crescimento de fibroblastos (especialmente TGF-Beta). Sua identificação abre um novo caminho para o tratamento do pterígio.
Resumindo, radiação ultravioleta e microtraumatismos, induzem uma processo inflamatório crônico, com perda da função de barreira do limbo córneo-conjuntival. A proliferação fibrovascular ocorre, remodelação do tecido conjuntivo, angiogênese e invasão da córnea.

Cirurgia de Pterígio
El o tratamento clássico é cirúrgico, ou seja, você tem que fazer um operação de pterígio com atenção especial para a região da córnea, a cabeça do pterígio. Quando o tamanho é pequeno, após sua extirpação basta suturar as bordas da conjuntiva saudável mas quando são tamanho ou tipo maior recaída, uma implante conjuntivalde membrana amniótica ou células-tronco cultivadas.
Este procedimento é eficaz em um alto grau de casos mas ainda há um alto percentual de recidivas que tornam necessária uma nova cirurgia. Não é bem conhecido causa de recorrências mas tudo sugere que algum grau de reação inflamatória persiste e uma cama no limbo que facilita nova proliferação fibrovascular e invasão da córnea, além da persistência do fator causal, a radiação ultravioleta, por ele É necessário avaliar esses três fatores.
Há muitas pessoas que relutam em se submeter à cirurgia de pterígio e por isso se perguntam:como remover pterígio sem cirurgia?. Quando o pterígio é pequeno o oftalmologista pode recomendar esteróides para reduzir a inflamação ou gotas para pterígio.
Os tres fatores-chave para o sucesso da cirurgia de ptreigion são:
Vídeo de operação do pterígio passo a passo Área Oftalmológica Avanzada
Antes da cirurgia
Proteção contra radiação ultravioleta
Em primeiro lugar, é óbvio que devemos proteger os olhos contra os raios ultravioleta, Os pacientes devem ser encorajados a evitar esse tipo de radiação, seja reduzindo sua exposição ou usando óculos de proteção., tendo o cuidado de escolher a armação certa e o filtro UV com potência suficiente.
durante a cirurgia
Cirurgia seletiva e reconstrução da conjuntiva
O terceiro fator, evitar o pterígio recorrenteenvolve tomar uma série de medidas cirúrgicas. A técnica de a remoção deve ser cuidadosa, dissecando todo o Pterígio, corpo e cabeça, todo o triângulo deve ser removido. O corpo é constituído por um epitélio conjuntival alterado que não deve ser preservado e um tecido conjuntivo fibrovascular que deve ser completamente removido.
La A cabeça do pterígio deve ser dissecada na córnea, atingindo seus planos profundos e removendo-a toda. É essencial que a superfície corneana e límbica é regular e lisa, pois caso contrário, sabemos que é um fator que facilitará o avanço do tecido fibrovascular da conjuntiva, iniciando a recidiva. Para isso é necessário usar instrumentos que “polirem” a superfície, uma broca de pó de diamante ou o aerorotor Barraquer.
Uma vez que o tecido anormal foi removido, devemos avaliar a possibilidade de fechar as bordas da conjuntiva saudável. Se possível usamos suturas que não induzem inflamação, como o nylon, já que os usuais como o vicryl, do tipo reabsorvível, podem facilitar a neoformação fibrovascular. Quando a área desnudada não pode ser ocluída pela aproximação das bordas da conjuntiva, é necessário um enxerto para garantir o efeito de barreira.
quando possível um autoenxerto de conjuntiva do mesmo olho é preferível, geralmente da região temporal superior e, se não houver tecido suficiente nesse olho, pode ser obtido do olho contralateral, sempre tendo o cuidado de obter células límbicas saudáveis que garantam a regeneração da área. Outra opção é o Implantação de células-tronco cultivadas ex vivo em suporte de membrana amniótica (22) Ele enxerto lata ser suturado ou fixado por substâncias aderentes, como fibrina (tisucol MT).
Depois da cirurgia
Inibição da reação inflamatória local
O segundo fator, reação inflamatória, tem que tomar medidas pré-operatórias, intra-operatórias e pós-operatórias.
Antes da intervenção é necessário o administração de anti-inflamatóriosou esteróides tópicos ou infiltração prévia de anti-VGF. foram descritos bons resultados com esta manobra, tanto na incidência de recidivas em recuperação após a cirurgia. No intraoperatório, recomenda-se aplicar drogas que inibem a proliferação de fibroblastos, como a Mitomicina C. Estudos comprovam a eficácia desta droga, sua aplicação a 0.02%, por 30 segundos, apresenta resultados muito bons (19). Outros medicamentos, como Tiotepa ou 5-Fluorouracil (20), não mostraram o mesmo nível de eficácia.
No pós-operatório também é necessário controlar a inflamação, principalmente nas fases iniciais, por isso é necessário administrar esteróides tópicos, até mesmo a instilação de Mitomicina C na forma de colírio tem sido proposta em casos complexos, onde é previsível uma possível recorrência. Talvez o A diretriz mais recomendada atualmente na prevenção da recorrência ou, quando vemos que se inicia, seria com infiltração de anti-VGF na área de risco (21).
Referências
1.- Arenas Archila E. Etiopatogenia de Pinguecula e Pterígio. Palestra Oftalmológica Panamericana 1978; 2(3):28
2.-Anyanwu E. Nnadozie JN. A distribuição de frequência de doenças oculares por idade em Imo Satate Nigéria. J Am OptomAssoc 1993, 64: 704.
3.- Cameron ME. Pterígio em todo o mundo. Springfield II. Charles C Thomas 1965.
4.-Goldberge L Davis R. Pterygium e sua relação com o olho seco no Bantu. Brit J Ohptalmol 1976, 60: 720.
5.- McKenzie FD, Hirst LW, et al. Análise de risco no desenvolvimento de pterígio. Oftalmologia 1992, 99: 1056.
6.-Threifall TJ, Inglês DR. Exposição solar e Pterígio do olho. Uma curva de dose-resposta Am J Ophthalmol 1999, 128: 280.
7.-Throutbeck R. Revisão do tratamento de pterígio em Queensland, 10 anos de cirurgia primária. Clin Experimento Ophth. 2001, 29: 286.
8.-Kwok LS, Coroneo MT. Um modelo de formação de Pterígio. Cornea 1994, 13: 219.
9.- Ansari MV, Rahi AHS et al. Natureza pseudoelástica do Pterígio. Br J Oftalmol 1970, 54: 473.
10.- Austin P. Jakobiec FA. Elastodisplasia e elastodistrofia como bases atológicas do pterígio e pinguécula ocular. Oftalmologia 1983.90:96.
11.-Dushku N, Reid TW. Expressão de P53 em células basais límbicas alteradas em pinguéculas, pterígios e tumores límbicos. Curr Eye Res 1997, 16: 1179.
12.- Ueda Y, Kanazawa S et al. Estudo imuno-histoquímico de p53, p21 e PCNA em pterígio. ActaHistochem, 2001: 103: 159.
13.-Luthra R, Nemesure BB et ai. Frequência e fatores de risco para pterígio no estudo do olho de Barbados. Arch Ophthalmol 2001, 119:1827.
14.- Li ZY, Wallace RN et al. Componentes de fibras elásticas e inibidores de protease em pinguécula. Invest Oftalmol Vis Sci 1991, 32: 1573.
15.-Dushka N, Hatcher SLS et al. p53 Expressão e relação com a infecção pelo papillonavirus humano em pinguéculas, pterígios e tumores límbicos. Arco Oftalmol 9199.117: 1593.
16.- Li DQ, Lee SB. et ai. Superexpressão de colagenase (MMP-1) e estromelisina (MMP-3) pelo fibroblasto da cabeça do pterígio. Arch Ophthalmol 2001, 119:71.
17.- Di Girolano N, Coroneo MT et al. Matrilisina ativa (MMP-7) em pterígio humano. Papel potencial da angiogênese. Invest Oftalmol Vis Sci 2001. 42: 1993.
18.- Cameron ME. Histologia do pterígio: um estudo microscópico eletrônico. Br J Ohthalmol 1983, 67: 604.
19.-FruchtPery J, Islar M. et ai. Dose única de mitomicina C para prevenção de pterígio recorrente. Córnea 1994, 13: 411.
20.-Pikkel J, Interrompendo a recorrência do pterígio por 5-fluorouracil pós-operatório. Córnea 2001, 20: 168.
21.-Hamid Hosseini, MD, Mohammad H. Terapia Anti-VEGF com Bevacizumab para Doença do Segmento Anterior do Olho. Córnea 2012;31:322
22.- Salomon A, Pires RT, Tseng SC. Transplante de membrana anmiótica após extensa remoção de pterígio primário e recorrente. Oftalmologia 2001, 108:449.


